Das Spin-off-Projekt “ContiVir” am Max-Planck-Institut für Dynamik komplexer technischer Systeme in Magdeburg, hat in der Fachzeitschrift Human Gene Therapy Ergebnisse veröffentlicht, in denen die Aufreinigung des Adeno-assoziierten Virus (AAV) mithilfe der membranbasierten sterischen Ausschlusschromatographie (SXC) detailliert beschrieben wird. Diese Technologie wurde von Dr.-Ing. Pavel Marichal-Gallardo, Forschungsgruppe Bioprozesstechnik, unter der Leitung von Prof. Dr.-Ing. Udo Reichl entwickelt.
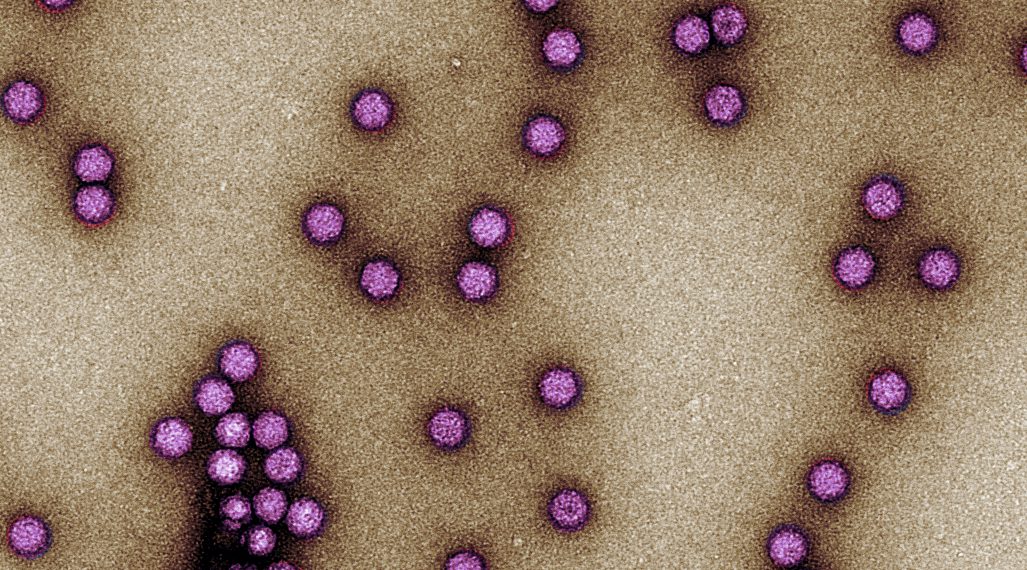
Viren können als Vektoren (Vehikel) für die Genabgabe verwendet werden, um mehrere angeborene oder erworbene Krankheiten beim Menschen zu behandeln (Bild 1). Für eine effiziente Therapie werden sie jedoch in sehr großen Mengen benötigt. Der Mangel an Produktionskapazitäten für die große Menge an Viruspartikeln, die für eine einzelne Behandlung erforderlich sind, ist ein bekannter Engpass, der von mehreren Branchenexperten und biopharmazeutischen Unternehmen öffentlich geäußert wird.
Obwohl die Zulassung der ersten Zell- und Gentherapien erst in den letzten Jahren erfolgt ist, stützt sich die industrielle Herstellung dieser Produkte immer noch auf Technologien, die älter als 30 Jahre sind und häufig niedrige Produktausbeuten und sogar das Risiko von Chargenfehlern aufweisen. Es ist davon auszugehen, dass die Zahl von Gentherapien, die in den nächsten Jahren zugelassen werden, wächst. Darüber hinaus wird die Weltbevölkerung immer größer und schwerwiegende Bedrohungen für die öffentliche Gesundheit wie COVID-19 werden die biopharmazeutische Lieferkette stark stören. Angesichts dieser Entwicklungen sind sich Experten einig, dass die schrittweise Erhöhung der Produktionskapazitäten mit aktuell verfügbaren Technologien nicht ausreicht, um die enorme Nachfrage nach Virenherstellung zu befriedigen. Neue, hocheffiziente Technologien, die diese Probleme angehen, werden dringend benötigt.
Höhere Geschwindigkeiten und Ausbeute, Plug-and-Play- und Einwegbetrieb dank innovativer chromatographischer Trenntechnik
Dr. Julian Lopez, verantwortlich für die Geschäftsentwicklung des ContiVir-Projekts, beschreibt die Neuerungen: „Unsere SXC-Technologie weist viele der Eigenschaften auf, die die Gentherapieindustrie wünscht, wenn sie neue Wege sucht, um aktuelle und zukünftige Herausforderungen bei der Herstellung von Viruspartikeln wirklich anzugehen, zum Beispiel höhere Geschwindigkeiten, höhere Ausbeute sowie Plug-and-Play- und Einwegbetrieb. SXC ist eine innovative chromatographische Trenntechnik (Steric Exclusion Chromatography, SXC).
“Unsere Ergebnisse unterstreichen die Vielseitigkeit von SXC als Plattformtechnologie für mehrere AAV-Varianten, unabhängig von ihren Oberflächeneigenschaften, die möglicherweise die Prozessentwicklung, das Scale-up und den Betrieb verkürzen und vereinfachen. In einigen Fällen konnten wir mit dem kleinsten SXC-Gerät eine Menge an AAV-Partikeln, die 20 gentherapeutischen Behandlungen der Netzhaut entspricht, in weniger als einer Stunde aus einer Zellfraktion gewinnen. In vielen Laboren wird diese häufig verworfen, weil sie nicht in der Lage sind, größere Mengen zu verarbeiten. Mit SXC muss dieses Material nicht verschwendet werden. Wir haben auch einen zehnmal schnelleren Prozess im Vergleich zu anderen derzeit verwendeten Aufreinigungsmethoden beobachtet.“
— Dr. Pavel Marichal-Gallardo
Prof. Grimm und Dr. Kathleen Börner, gleichberechtigte Erstautorin dieser Studie und leitende Wissenschaftlerin bei Prof. Dr. med. Hans-Georg Kräusslich am Universitätsklinikum Heidelberg, fügen hinzu: “Wir freuen uns besonders, dass diese neue Technologie sowohl mit häufig verwendeten AAV-Wildtypen als auch mit synthetischen Designer-AAV-Kapsidvarianten kompatibel ist. Diese werden von uns und unseren Kollegen ständig weiterentwickelt. SXC ist für die Verfügbarkeit universeller und skalierbarer Aufreinigungswerkzeuge und deren erfolgreiche Anwendung in der Gentherapie beim Menschen von entscheidender Bedeutung.”
Gegenwärtig wird die membranbasierte SXC-Technologie von mehreren Partnern aus der Industrie getestet, die von ContiVir optimierte Prototypen im Labormaßstab erhalten haben. Sie ähneln denen, die in der kürzlich veröffentlichten Arbeit in Human Gene Therapy zur Aufreinigung von AAV-Partikeln verwendet wurden (Bild 2).
Julian Lopez erklärt weiter: „In den letzten Monaten konnten wir ein verstärktes Interesse an unserer SXC-Technologie feststellen. Wir haben jetzt zwei SXC-Prototypen in unserem Forschungsportfolio (Bild 3), damit unsere Partner uns Feedback geben können, um das Produkt so zu verbessern, dass es ihren Anforderungen und Erwartungen entspricht. Wir beabsichtigen, in den nächsten Monaten mehrere SXC-Modelle zu haben, die für die Herstellung von klinischem Material geeignet sind – ein Schlüsselmerkmal, das von immer mehr Partnern gefordert wurde.“
Die Forschung von ContiVir wird von der Europäischen Union und der Bundesregierung im Rahmen des EXIST Forschungstransfer-Programms finanziert. Die Laboreinrichtungen von ContiVir befinden sich am Lehrstuhl für Bioverfahrenstechnik an der Otto-von-Guericke-Universität Magdeburg.